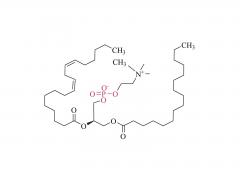
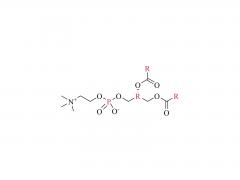
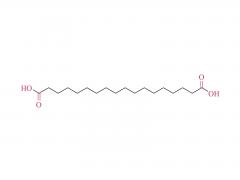
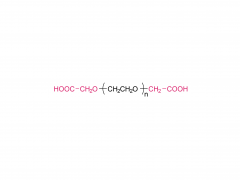
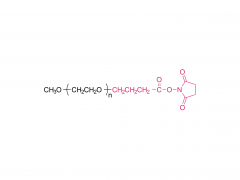
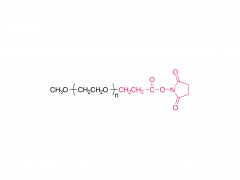
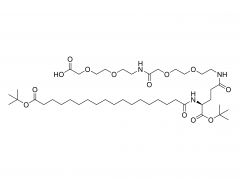
J Biotechnologie. 31 décembre 2012;162(2-3):283-8. est ce que je: 10.1016/j.jbiotec.2012.09.008. Publication en ligne du 20 septembre 2012. Préparation, analyse structurale et bioactivité du conjugué ribonucléase A-albumine : tétra-conjugaison ou PEG comme lieur Résumé La ribonucléase A (RNase A) est une enzyme thérapeutique ayant une action cytotoxique contre les cellules tumorales. Son application clinique est limitée par sa demi-vie courte et sa stabilité insuffisante. La conjugaison de l'albumine peut surmonter cette limitation, tout en diminuant considérablement l'activité enzymatique de la RNase A. Ici, trois stratégies ont été proposées pour préparer les conjugués RNase A-albumine sérique bovine (BSA). Le R-SMCC-B (un conjugué de quatre RNase A attachées à une BSA) et le R-PEG-B (un monoconjugué) ont été préparés en utilisant du Sulfo-SMCC (un court lieur bifonctionnel) et du mal-PEG-NHS (un bifonctionnel PEG), respectivement. Le mal-PEG-NHS et l'hexadécylamine (HDA) ont été utilisés pour préparer le mono-conjugué R-HDA-B, où la HDA a été adoptée pour lier la BSA. Le lieur PEG peut allonger la proximité entre la RNase A et la BSA. En revanche, quatre RNase A étaient étroitement localisées sur la BSA dans le R-SMCC-B. R-SMCC-B a montré le K(m) le plus faible et l'activité enzymatique relative la plus élevée et k(cat)/K(m) dans les trois conjugués. Vraisemblablement, l'interaction tétravalente de la RNase A dans R-SMCC-B peut augmenter l'affinité de liaison avec son substrat. De plus, la libération lente de BSA par le R-HDA-B peut augmenter l’activité enzymatique du R-HDA-B. Notre étude devrait fournir des stratégies pour développer un conjugué protéine-albumine à fort potentiel thérapeutique. Pour plus d'informations sur le produit, veuillez nous contacter à : Tél. aux États-Unis : 1-844-782-5734 Tél. aux États-Unis : 1-844-QUAL-PEG CHN Tél. : 400-918-9898 E-mail : sales@sinopeg.com
Afficher plus