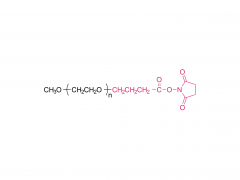
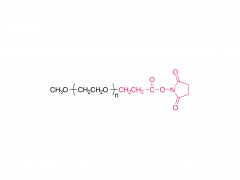
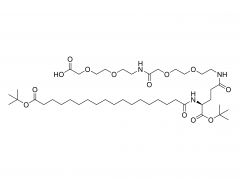
Bioact Mater. 2024 juin 21:40:430-444. doi: 10.1016/j.bioactmat.2024.06.021. eCollection 2024 oct. Hydrogel malléable de type pâte se transformant d'un réseau dynamique en un réseau rigide pour réparer les défauts osseux irréguliers Abstrait Les défauts osseux irréguliers, caractérisés par une taille, une forme et une profondeur imprévisibles, représentent un défi majeur pour le traitement clinique. Bien que diverses greffes osseuses soient disponibles, aucune ne permet de répondre pleinement aux besoins de réparation de la zone lésée. Cette étude décrit la fabrication d'un hydrogel de type pâteux (DR-Net), dont le premier réseau dynamique est généré par la coordination entre les groupes thiol et les ions argent, lui conférant ainsi la malléabilité nécessaire pour s'adapter à divers défauts osseux irréguliers. Le second réseau covalent rigide est formé par photoréticulation, maintenant l'espace ostéogénique sous l'effet de forces externes et optimisant l'adéquation au processus de régénération osseuse. In vitro, un défaut osseux alvéolaire irrégulier est créé dans une mandibule de porc fraîche, et l'hydrogel de type pâteux présente une remarquable adaptabilité de forme, épousant parfaitement la morphologie du défaut osseux. Après photopolymérisation, le module de conservation de l'hydrogel est multiplié par 8,6, passant de 3,7 kPa (avant irradiation) à 32 kPa (après irradiation). De plus, cet hydrogel permet un chargement efficace du peptide P24, qui accélère fortement la réparation osseuse chez les rats Sprague-Dawley (SD) présentant des défauts crâniens critiques. Globalement, cet hydrogel de type pâteux, malléable, capable de maintenir l'espace et doté d'une activité ostéogénique, présente un potentiel exceptionnel pour une application clinique dans le traitement des défauts osseux irréguliers. Mots-clés : Hydrogel de type pâte ; Réseau dynamique ; Défaut osseux irrégulier ; Malaxable ; Réseau rigide. Produit: Fabricant de dérivés de PEG par structure, grossiste de dérivés de PEG par structure
Afficher plus