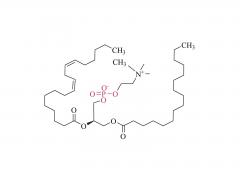
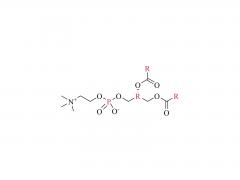
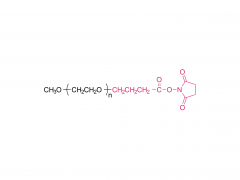
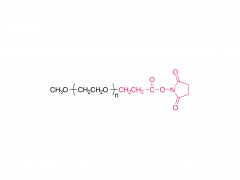
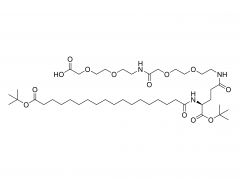
Langmuir. 1er juillet 2014 ;30(25) :7465-74. doi : 10.1021/la500403v. Publication en ligne le 17 juin 2014. Effet des espaceurs polyéthylène glycol, alkyle et oligonucléotidique sur la liaison, la structure secondaire et l'auto-assemblage des aptamères-amphiphiles FKN-S2 liant la fractalkine Abstrait Nous avons précédemment identifié un aptamère, nommé FKN-S2, qui se lie à la protéine de surface cellulaire fractalkine avec une affinité et une spécificité élevées. Dans cet article, une queue dialkyle hydrophobe en C16 a été ajoutée à l'aptamère pour créer un aptamère-amphiphile. Nous avons étudié comment la queue et une molécule espaceur de longueur et d'hydrophobicité variables, insérée entre la queue et la tête de l'aptamère, affectent la liaison, la structure et les propriétés d'auto-assemblage de l'aptamère-amphiphile. Nous avons synthétisé des aptamères-amphiphiles sans espaceur (NoSPR), avec des polyéthylène glycols (PEG4, PEG8, PEG24), des alkyles (C12 et C24) ou des oligonucléotides (T10 et T5 : 10 et 5 thymine, et A10 : 10 adénine). L'ajout de la queue a réduit l'affinité de liaison de l'aptamère-amphiphile de plus de 7,5 fois par rapport à l'aptamère libre. Les espaceurs alkyles hydrophobes ont entraîné la plus forte perte d'affinité, tandis que les espaceurs PEG hydrophiles ont amélioré l'affinité amphiphile, sans toutefois la restaurer à celle de l'aptamère libre. Il est intéressant de noter que les espaceurs oligonucléotidiques ont produit les amphiphiles présentant la plus forte affinité. La composition nucléotidique n'a cependant pas affecté l'affinité, les espaceurs T10 et A10 ayant une affinité égale. Les amphiphiles de l'espaceur oligonucléotidique présentaient la plus forte affinité, car l'espaceur oligonucléotidique augmentait l'affinité de l'aptamère libre ; l'aptamère FKN-S2 associé à l'espaceur oligonucléotidique présentait une affinité supérieure à celle de l'aptamère FKN-S2 libre. La spectroscopie de dichroïsme circulaire (CD) et les études de fusion thermique ont indiqué que l'aptamère forme un G-quadruplexe tige-boucle et intramoléculaire, et que la queue stabilisait fortement la formation du G-quadruplexe dans un tampon. L'imagerie par microscopie électronique à transmission cryogénique (cryo-TEM) a montré que les aptamères-amphiphiles, indépendamment de l'espaceur utilisé, s'auto-assemblaient en micelles et nanorubans, structures bicouches plates souvent torsadées. Enfin, des liposomes fonctionnalisés avec l'amphiphile FKN-S2 ont été incubés avec des cellules exprimant la fractalkine, et le degré de liaison dépendait de la concentration de l'amphiphile à la surface des liposomes.
Afficher plus