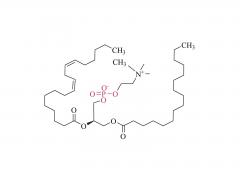
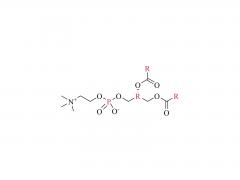
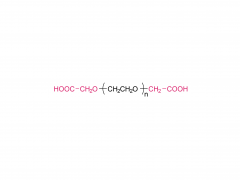
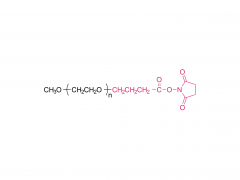
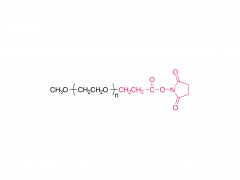
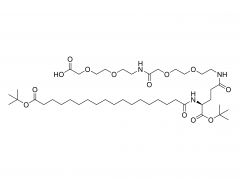
Bioconjugué Chem. 21 juillet 2021;32(7):1263-1275. est ce que je: 10.1021/acs.bioconjchem.1c00172. Publication en ligne le 30 mai 2021. L'influence d'un lieur polyéthylèneglycol sur le métabolisme et la pharmacocinétique d'un anticorps radiomarqué au 89Zr Résumé La plupart des travaux expérimentaux dans le domaine de la chimie de la bioconjugaison se concentrent sur l'utilisation de nouvelles méthodes pour construire des liaisons covalentes entre une molécule cargo et une protéine d'intérêt telle qu'un anticorps monoclonal (mAb). La formation de liaisons est importante pour générer de nouveaux outils de diagnostic, mais lorsque ces composés progressent vers des études précliniques in vitro et in vivo, puis pour leur traduction en clinique, il est important de comprendre le sort des métabolites potentiels résultant de la dégradation chimique ou enzymatique de la construction. pour obtenir une image complète des performances pharmacocinétiques d’un nouveau composé. Dans le cadre de la conception de nouvelles méthodes de bioconjugués pour le marquage des anticorps avec le radionucléide émetteur de positrons 89Zr, nous avons précédemment développé un procédé photochimique pour fabriquer des 89Zr-mAbs. Des études expérimentales sur les constructions [89Zr] ZrDFO-PEG3-azépine-mAb ont révélé que l'incorporation du lieur tris-polyéthylène glycol (PEG3) améliorait la solubilité de la phase aqueuse et la conversion radiochimique. Cependant, l'utilisation d'un lieur PEG3 a également un impact sur le temps de séjour de la construction dans tout le corps, conduisant à une excrétion plus rapide de l'activité 89Zr par rapport aux radiotraceurs dépourvus de la chaîne PEG3. Dans ce travail, nous avons étudié le devenir métabolique de huit métabolites possibles résultant de la déconnexion logique du [89Zr] ZrDFO-PEG3-azepin-mAb au niveau de liaisons sensibles au clivage chimique ou enzymatique. La synthèse combinée au radiomarquage au 89Zr, à l'imagerie par tomographie par émission de positrons sur petits animaux à plusieurs moments de 0 à 20 h et aux mesures de la demi-vie efficace pour l'excrétion du corps entier est rapportée. Les conclusions sont que l’utilisation d’un lieur PEG3 n’est pas innocente en termes de son impact sur l’amélioration du métabolisme des [89Zr]ZrDFO-PEG3-azepin-mAbs. Dans la plupart des cas, la dégradation peut produire des métabolites qui sont rapidement éliminés du corps, améliorant ainsi le contraste de l'image en réduisant l'accumulation non spécifique et la rétention de 89Zr dans les organes de fond tels que le foie, la rate, les reins et les os. Pour plus d'informations sur le produit, veuillez nous contacter à : Tél. aux États-Unis : 1-844-782-5734 Tél. aux États-Unis : 1-844-QUAL-PEG CHN Tél. : 400-918-9898 E-mail : sales@sinopeg.com
Afficher plus