#ASOs #oligonucléotide antisens #GalNAc #livraison de médicaments #ciblage de ligand
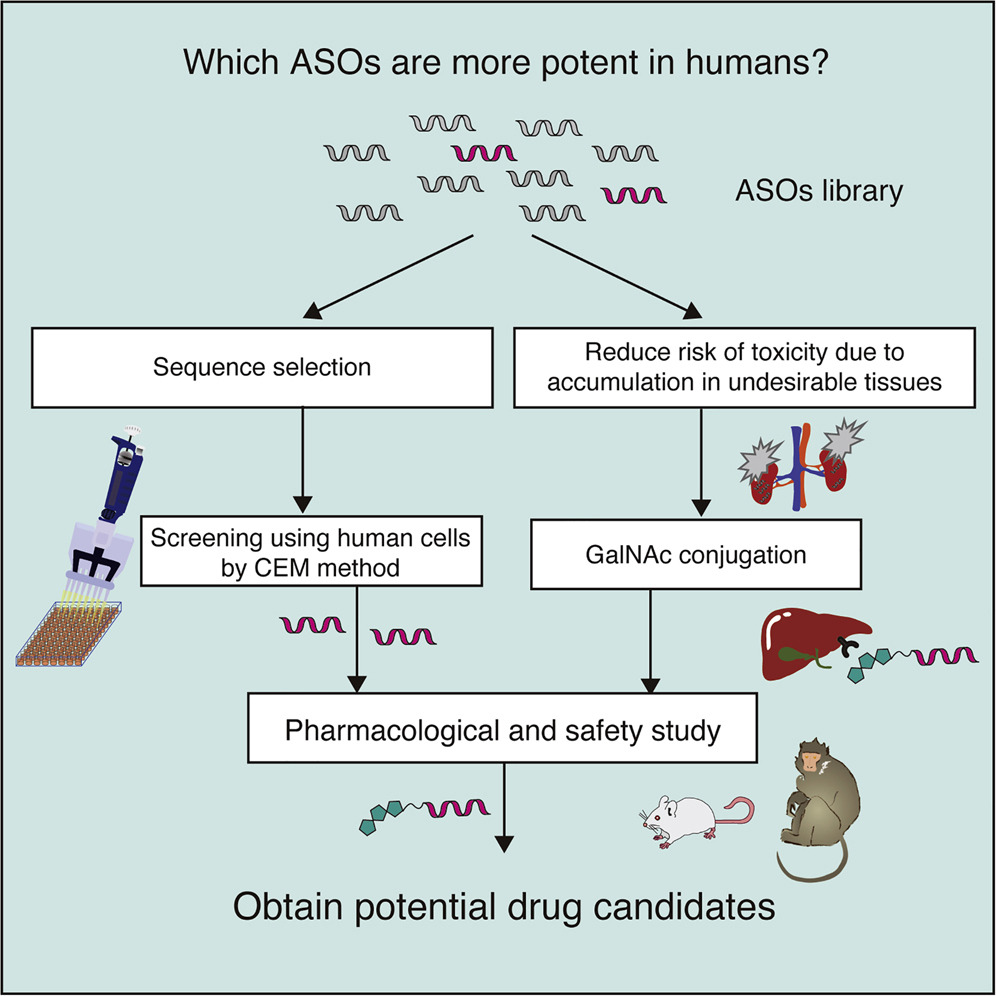
Le schéma de développement de médicaments utilisant le conjugué GalNAc est mieux adapté à la sélection d'ASO à base de BNA, en particulier pour le traitement des maladies associées au foie.
 grandeur
grandeur
https://www.cell.com/molecular-therapy-family/molecular-therapy/fulltext/S1525-0016(22)00428-2
Les oligonucléotides antisens (ASO) contenant des acides nucléiques pontés (BNA) se sont avérés très puissants. Cependant, il reste un défi pour assurer une découverte fiable et un schéma de développement translationnel pour cette classe d'ASO avec des fenêtres thérapeutiques plus larges. La robustesse du schéma a été démontrée dans le cadre de la sélection des ASO, qui ont deux chimies différentes de BNA (2,′4′-BNA/acide nucléique verrouillé [LNA] et acide nucléique à pont amido [AmNA]) ciblant la proprotéine humaine convertase subtilisine/kexine de type 9 (PCSK9). Un processus en deux étapes a été mis en place, comprenant une approche de criblage in vitro unique et sensible, appelée transfection d'enrichissement en milieu de Ca2+ (CEM), et une approche d'administration de médicaments ciblée sur les ligands pour mieux atteindre les tissus cibles, évitant ainsi l'accumulation involontaire d'ASO. Un ligand N-acétylgalactosamine (GalNAc) a ensuite été ajouté au candidat ASO pour élargir encore la marge thérapeutique en modifiant la pharmacocinétique de la molécule. Avec une néphrotoxicité réduite chez les rats, le conjugué GalNAc, HsPCSK9-1811-LNA, s'est avéré au moins dix fois plus puissant chez les primates non humains. Dans l'ensemble, un schéma de développement de médicaments s'est avéré mieux adapté à la sélection d'ASO à base de BNA cliniquement pertinents, en particulier pour le traitement des maladies associées au foie.