Les copolymères séquencés constituent une classe impérative de systèmes multiphasiques qui sont devenus des matériaux importants au cours des dernières années et ont suscité un intérêt mondial auprès des physiciens, des chimistes, des biologistes et des ingénieurs chimistes, et ont été largement utilisés en médecine, en construction et en chimie. industrie. Les copolymères blocs sont composés d'homopolymères chimiquement différents reliés de manière covalente à une extrémité, chaque polymère de copolymère bloc peut être appelé bloc. L'une des propriétés les plus intéressantes des copolymères séquencés est leur capacité à s'auto-assembler en structures de microdomaines ordonnées.
Les copolymères séquencés amphiphiles sont généralement linéaires (dibloc, tribloc et multibloc), cycliques et miktoarm. La nature chimique des blocs constitutifs, leur composition et leur poids moléculaire total présentent un comportement en solution varié et d'excellentes propriétés.
Les progrès actuels des copolymères séquencés sont fortement liés au développement de nouvelles techniques de polymérisation efficaces. Les copolymères séquencés peuvent généralement être obtenus par (a) une polymérisation séquentielle contrôlée ou vivante, (b) une simple réaction de couplage, (c) en utilisant un double initiateur de 2 fragments initiateurs différents, et (d) les macro-initiateurs incluant la commutation de fonctionnalité. Il convient de souligner que parfois, il est impossible de synthétiser des copolymères présentant une certaine structure souhaitée uniquement par une seule technique de polymérisation. Dans un tel cas, la combinaison de différentes techniques de synthèse et la fonction de changement de groupe sont des stratégies réalisables.

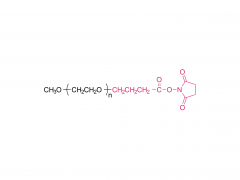
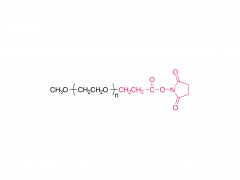
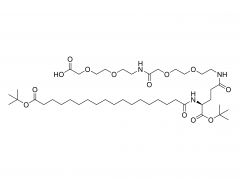
Le PEG est un polyéther hydrophile non ionique qui présente une excellente biocompatibilité et qui est approuvé par la FDA pour la consommation interne. Le PEG est un polymère neutre avec des groupes terminaux hydroxyle qui sont des acides à liaison hydrogène faible et des liaisons éther faiblement basiques dans le squelette. Les molécules PEG peuvent être ajoutées aux véhicules d'administration de médicaments via un certain nombre de voies différentes, notamment la liaison covalente, le mélange pendant la préparation ou l'adsorption en surface. Il peut être modifié à l'un ou l'autre des groupes terminaux pour être attaché à d'autres molécules ou polymères. Le PEG, qui a été introduit à l'origine dans le domaine pharmaceutique dans le but de prolonger la demi-vie des protéines dans le sang, de réduire leur immunogénicité et de les protéger de la dégradation protéolytique, est largement choisi pour développer des copolymères blocs en raison de son hydrophilie, sa linéarité, la flexibilité de sa chaîne, son absence de charge et sa disponibilité dans une large gamme de MW avec une distribution étroite de MW.
Un polymère biodégradable est considéré comme « vert » car il ne s'accumule pas dans le corps et ne nuit pas à l'environnement, ce qui montre son application intéressante dans le domaine biomédical ou de l'administration de médicaments en raison de sa capacité à être facilement métabolisé et excrété. le corps. Les matériaux biodégradables ne se limitent pas au ciblage spécifique d'un site de médicaments, de peptides et de protéines, mais sont également de plus en plus importants dans les dispositifs médicaux et les pansements. Pour répondre à ces exigences, les copolymères séquencés biodégradables ont été étudiés en tant que biomatériaux prometteurs en raison de leur capacité à modifier leur comportement amphiphile et leurs propriétés physiques et mécaniques en modifiant le rapport des blocs constitués ou en ajoutant de nouveaux blocs aux propriétés souhaitées.
Les copolymères séquencés existent sous forme d'unimères en dessous de leur concentration micellaire critique (CMC) et forment des assemblages macromoléculaires de type noyau-coquille sous forme de micelles polymères au-dessus de la CMC. Les micelles polymères résultantes formées sont en équilibre avec leurs unimères respectifs. La micellisation de ces polymères dans l'eau ressemble à l'auto-assemblage de tensioactifs. Les micelles polymères font partie des plates-formes d'administration largement étudiées où l'enveloppe externe minimise l'opsonisation et le noyau interne s'occupe de la solubilisation des médicaments, une condition préalable au transport des médicaments. La faible solubilité aqueuse des médicaments hydrophobes limite le taux de réussite lors du criblage à haut débit. Cela pose un défi pour la formulation des scientifiques, en particulier compte tenu du nombre croissant de molécules approuvées présentant un poids moléculaire, un point de fusion et une lipophilie élevés. L'approche traditionnelle de solubilisation dans les formulations à base de lipides souffre d'une précipitation rapide du médicament in vivo, avant son absorption. À l’inverse, les micelles présentent une stabilité thermodynamique et une biocompatibilité supérieures.

Récemment, l'intérêt des chercheurs s'est porté sur l'application de micelles de copolymères séquencés comme système de nanoporteurs dans le domaine de l'administration de médicaments en raison de la capacité hydrophobe de chargement de médicaments du noyau interne ainsi que des caractéristiques uniques de disposition in vivo. Ces micelles de copolymères séquencés offrent de nombreux avantages en tant que systèmes d'administration de médicaments efficaces, notamment (1) une préparation facile, (2) une stabilité colloïdale avec une faible concentration micellaire critique (CMC), (3) des tailles réglables avec une distribution de taille étroite, (4) la capacité de protéger médicaments contre une éventuelle désactivation et préserver leurs activités pendant la circulation et le trafic intracellulaire, (5) une pharmacocinétique améliorée et (6) une efficacité de chargement physique élevée des médicaments sans modification chimique.
Plusieurs polymères plastiques biodégradables, tels que le polyéthylène glycol (PEG), l'acide polylactique (PLA), la polycaprolactone (PCL) et leurs copolymères séquencés, ont été développés pour des applications biomédicales. En tant qu'objet de recherche ces dernières années, le copolymère bloc polyéthylène glycol-acide polylactique (PEG-PLA) et ses nanoparticules dérivées du groupe terminal peuvent améliorer la charge de médicaments hydrophobes, réduire l'effet d'éclatement, éviter d'être engloutis par les phagocytes, augmenter la circulation. temps de médicaments dans le sang et améliorer la biodisponibilité.
La chimiothérapie conventionnelle manque de ciblage spécifique sur la tumeur, ce qui entraîne l'émergence de plusieurs cas d'exposition aux médicaments des cellules saines et de résistance aux médicaments. En outre, la faible solubilité aqueuse des médicaments anticancéreux constitue un facteur limitant dans la conception des médicaments. Les copolymères séquencés peuvent contourner ce problème en raison de leurs caractéristiques d’auto-assemblage et de leur efficacité élevée de chargement de médicament. Les propriétés physicochimiques réglables et la fonctionnalisation ultérieure constituent des excipients très prometteurs pour le développement de la formulation. Les micelles copolymères blocs subissent une distribution et une rétention passives au sein du site ciblé via un effet de perméabilité et de rétention amélioré. Il facilite le transport et la localisation des macromolécules ou des particules avec une exposition et des dommages minimes aux cellules saines.Par conséquent, ces nanoagrégats ont suscité une grande attention et un énorme optimisme en matière d'administration de médicaments et de thérapies ciblées, car ils sont thermodynamiquement stables, biocompatibles et moins toxiques. Néanmoins, la distribution des médicaments est hétérogène en raison de la non-uniformité du système vasculaire. Cependant, cette distribution peut être rendue plus spécifique grâce à une modification chimique du squelette polymère qui permet une interaction sélective et de haute affinité du support fonctionnalisé avec les cellules cibles.
Les micelles copolymères bloquées piègent le médicament lipophile dans son noyau de microenvironnement hydrophobe et améliorent sa solubilité et sa biodisponibilité. Leur auto-assemblage dépend de la différence de solubilité dans l'eau entre les blocs hydrophiles et hydrophobes. À mesure que la température augmente, le nombre d'association augmente progressivement, induisant ainsi une croissance micellaire anisotrope ou une transition structurelle. Des études ont également montré l'approche micellaire mixte qui combine généralement deux copolymères séquencés avec différentes valeurs d'équilibre hydrophile-lipophile afin d'améliorer l'encapsulation et la stabilisation du médicament.
En résumé, bles systèmes d'administration de médicaments à base de copolymères block présentent un grand potentiel pour améliorer l'efficacité des molécules thérapeutiques et minimiser leurs effets secondaires nocifs. Ainsi que leurs comportements d’auto-assemblage, qui sont d’une importance cruciale dans les domaines de la médecine, de la vie, de la biotechnologie et de l’environnement, et qui fourniront des applications inattendues.
Références
1. Kuperkar, K., Tiwari, S. et Bahadur, P. Nanoagrégats de copolymères blocs auto-assemblés pour les applications d'administration de médicaments. Applications des polymères dans l’administration de médicaments, 2021, 423–447. 10.1016/B978-0-12-819659-5.00015-X
2. Raval, N., Kalyane, D., Maheshwari, R. et Tekade, R. K. Copolymères et copolymères séquencés dans l'administration et la thérapie de médicaments. Fondements de base de l’administration de médicaments, 2019, 173–201. 10.1016/B978-0-12-817909-3.00005-4
3. Giram, P. S., Wang, J. T.-W., Walters, A. A., Rade, P. P., Akhtar, M., Han, S., Al-Jamal, KT Green synthèse de méthoxy-poly(éthylène glycol)-bloc-poly(l -lactide-co-glycolide) utilisant la proline de zinc comme initiateur biocompatible pour l'administration d'irinotécan au cancer du côlon in vivo. Science des biomatériaux. 2020. 10.1039/d0bm01421d